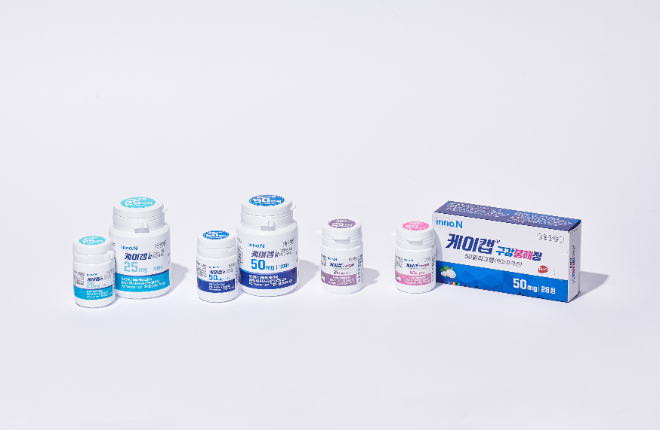
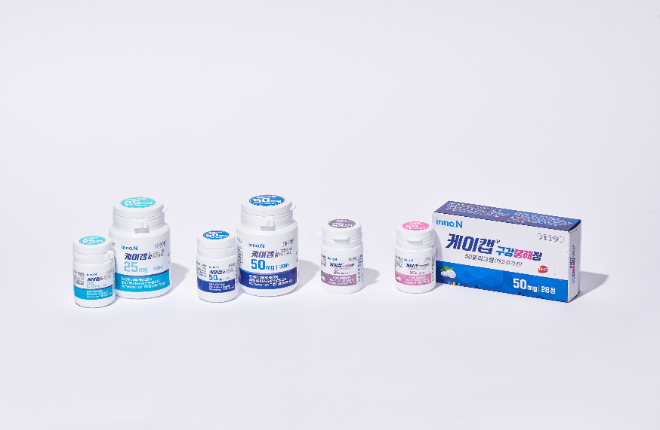
HK이노엔 위식도 역류질환 신약 '케이캡(성분명 테고프라잔)'이 미국 3상 임상을 성공적으로 마쳤다.
HK이노엔은 파트너사 세벨라가 23일(현지시간) 위식도 역류질환(GERD) 환자를 대상으로 테고프라잔(국내 제품명 케이캡)을 평가한 두 건의 미국 3상 임상시험 'TRIUMpH'의 주요 결과(톱 라인)를 발표했다고 24일 전했다.
이번에 톱 라인을 발표한 미국 3상 임상시험은 미란성 식도염(EE)과 비미란성 위식도 역류질환(NERD) 환자를 대상으로 실시했다. 미국 임상은 2021년 HK이노엔과 라이선스 계약을 체결한 미국 파트너사 세벨라의 소화기 의약품 전문 계열사 브레인트리가 진행했다.
미란성 식도염 및 비미란성 위식도 역류질환 임상 결과, 테고프라잔은 1차 및 2차 평가지표 모두 충족했다.
특히 미란성 식도염 임상에서는 미란성 식도염 전체 환자군과 중등도 이상의 식도염(LA 등급 C, D)환자군 모두의 2주 및 8주 차 치유율에서 기존 위산분비 억제제 PPI(란소프라졸) 대비 통계적 우월성을 입증했다.
비미란성 위식도 역류질환 임상시험에서 테고프라잔은 가슴쓰림(야간 및 가슴쓰림 없는 날)과 위산 역류 모두에서 완전한 증상 개선 효과가 확인됐다.
곽달원 HK이노엔 대표는 "대한민국이 개발한 신약 케이캡이 세계 최대 의약품 시장인 미국에서 성공적으로 3상 임상시험을 마쳐 매우 뜻깊게 생각한다"며 "세벨라 및 브레인트리와의 긴밀한 협업을 통해 앞으로도 테고프라잔이 미국을 포함한 글로벌 시장에서 위식도 역류질환 치료의 새로운 표준으로 자리 잡을 수 있도록 최선을 다할 것"이라고 밝혔다.
한편 세벨라는 이번 임상시험 외에 추가로 진행 중인 '미란성 식도염 치료의 유지 요법' 3상 임상시험을 올해 3분기에 마칠 예정이다.
4분기에는 미국 식품의약국(FDA)에 미란성 식도염 및 비미란성 위식도 역류질환 적응증을 포함한 신약 허가신청(NDA)을 제출할 계획이다.
김나영 한국금융신문 기자 steaming@fntimes.com































![최태원 SK 회장 '꼼수없는 경영' 어디서 배웠나 봤더니 [오너가 나온 그 대학]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2025042316461703656dd55077bc212411124362.jpg&nmt=18)
![비대면 대세라지만…신한은행, 점포 감소 '최대' [은행 공정금융 점검②]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2025021115324009674b4a7c6999c145616762.jpg&nmt=18)
![새마을금고중앙회, MG캐피탈에 2000억 유증…재무 안전성 강화 기대 [상호금융은 지금]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2024032421433509572dd55077bc22109410526.jpg&nmt=18)

![남기문 스마일게이트인베 대표, AUM 1.5조 코앞…올해 펀드 청산으로 성과보수 유입 기대 [2024 VC 실적]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2025042116092600869957e88cdd512116082156.jpg&nmt=18)
!["낮은 수익률 해결해야"…'퇴직연금 기금화' 도입 논의 깃발 [연금 통신]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2025042319404701810179ad439072211389183.jpg&nmt=18)












![[카드뉴스] KT&G ‘Global Jr. Committee’, 조직문화 혁신 방안 제언](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=202503261121571288de68fcbb3512411124362_0.png&nmt=18)


![[카드뉴스] 국립생태원과 함께 환경보호 활동 강화하는 KT&G](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=202403221529138957c1c16452b0175114235199_0.png&nmt=18)
![[카드뉴스] 신생아 특례 대출 조건, 한도, 금리, 신청방법 등 총정리...연 1%대, 최대 5억](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=20240131105228940de68fcbb35175114235199_0.jpg&nmt=18)
![[신간] 리빌딩 코리아 - 피크 코리아 극복을 위한 생산성 주도 성장 전략](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2025032814555807705f8caa4a5ce12411124362.jpg&nmt=18)
![[신간] 지속 가능 경영, 보고와 검증](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2025011710043006774f8caa4a5ce12411124362.jpg&nmt=18)
![[서평] 추세 매매의 대가들...추세추종 투자전략의 대가 14인 인터뷰](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2023102410444004986c1c16452b0175114235199.jpg&nmt=18)

![[신간] 똑똑한 금융생활...건전한 투자와 건강한 재무설계 지침서](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2025031015443705043c1c16452b012411124362.jpg&nmt=18)

![[카드뉴스] KT&G ‘Global Jr. Committee’, 조직문화 혁신 방안 제언](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=89&h=45&m=1&simg=202503261121571288de68fcbb3512411124362_0.png&nmt=18)
![[AD] 기아, 혁신적 콤팩트 SUV ‘시로스’ 세계 최초 공개](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=89&h=45&m=1&simg=2024123113461807771f9c516e42f12411124362.jpg&nmt=18)
![[AD] 아이오닉5 '최고 고도차 주행 전기차' 기네스북 올랐다...압도적 전기차 입증](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=89&h=45&m=1&simg=2024123113204707739f9c516e42f12411124362.jpg&nmt=18)




