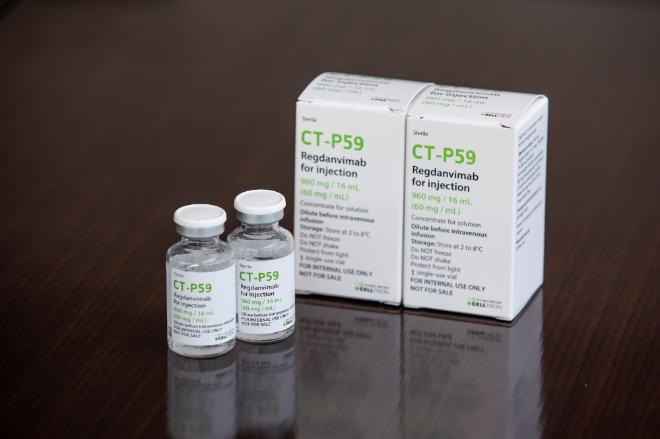
식품의약품안전처는 21일 법정 자문기구인 ‘중앙약사심의위원회’에서 ‘렉키로나주’의 안전성, 효과성, 허가 시 고려해야 할 사항 등에 대해 오는 27일 자문받고, 그 결과를 당일 공개할 예정이라고 밝혔다.
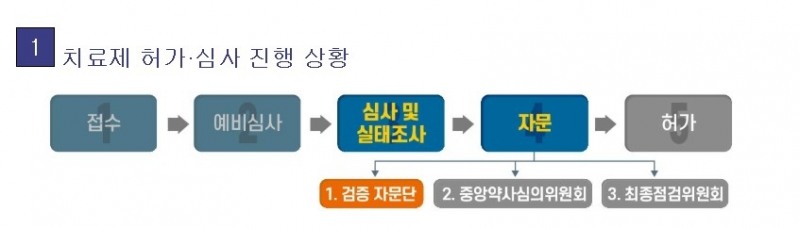
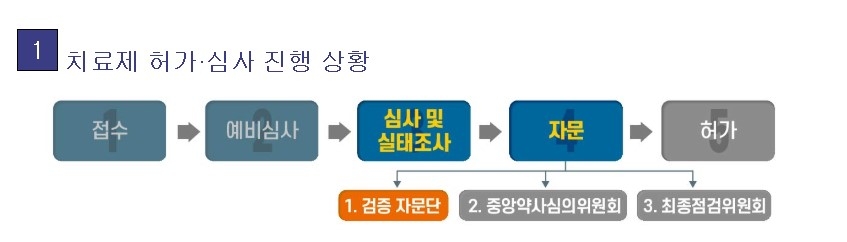
중앙약사심의위원회 자문은 코로나19 치료제 허가 과정에서 거쳐야 하는 세 번의 자문 절차 가운데 두 번째 과정이다. 지난 18일 식약처 검증 자문단은 ‘렉키로나주’의 3상 임상시험 수행을 전제로 품목허가를 제안했다.
식약처는 전날(20일) 셀트리온에 ‘렉키로나주’와 관련해 아직 제출되지 않은 품질자료 일부 등에 대한 자료 제출을 요청했다며, 제출되는 대로 심사를 계속 진행할 예정이라고 전했다.
식약처는 ‘렉키로나주’와 관련해 제조소 및 임상시험실시기관(의료기관)에 대한 실태조사는 마쳤다. 또한, 임상 시험 전반에 걸쳐 규정 준수 여부를 서류검토 및 현장 점검을 통해 임상시험 참여 환자의 안전과 시험 결과의 신뢰성을 확인했다. 해외 의료기관의 경우 임상시험의 신뢰성과 국제적 윤리기준에 따라 수행됐는지 서류상으로 중점 검토했다.
식약처는 현재 비임상·임상시험 자료에 대한 추가 검토와 품질자료에 대한 심사를 진행하고 있다. 유전자재조합의약품의 특성을 고려한 원료관리 자료, 공정단계별 불순물 제거 검증 자료, 보관 방법 및 사용 기간 설정을 위한 안정성시험 자료도 검토 중이다.
식약처는 코로나19 백신인 ‘아스트라제네카코비드-19 백신주’와 관련된 실태조사도 마쳤다. 이들은 지난 15일 비임상·임상시험 자료와 품질자료 등 심사에 필요한 자료를 추가로 요청했다.
‘아스트라제네카코비드-19’와 관련해 외부 전문가들이 참여하는 ‘코로나19 백신 안전성·효과성 검증 자문단’ 회의는 오는 31일에 실시하고, 내달 1일 발표할 예정이다.
식약처 측은 “자료가 제출되는 대로 예방효과, 신청한 용법‧용량의 타당성, 안전성 등에 대해 검토하고, 국가출하승인을 위한 품질 분야 심사에 집중할 예정”이라고 말했다.
정은경 기자 ek7869@fntimes.com




























![박기호 LB인베 대표, '3조' 기업가치 에이블리·펀드 청산으로 영업이익 증가 [2024 VC 실적]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=20250123191400059018a55064dd159679229.jpg&nmt=18)
!['尹 파면'에 롤러코스터 탄 코스피…"증시 불확실성 해소 국면 진입" [尹 파면]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2025040412325801343179ad439072112358872.jpg&nmt=18)


![트럼프發 관세 파장…증권사들이 바라본 코스피 전망과 투자 전략은? [美 관세 쇼크]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2023122100270607026c1c16452b018222889185.jpg&nmt=18)

![美 증시, 트럼프표 '공격적' 관세에 패닉 셀…애플 '털썩' M7 주가 타격 [美 관세 쇼크]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=20230803092941058129249a1ae63175114235199.jpg&nmt=18)
![대통령 파면 소식에 외국인 1조7천억원 매도…삼전 2.6%↓·하이닉스 6%↓(종합) [尹 파면]](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2025040411285401558e41d7fc6c2596154205.jpg&nmt=18)













![[카드뉴스] KT&G ‘Global Jr. Committee’, 조직문화 혁신 방안 제언](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=202503261121571288de68fcbb3512411124362_0.png&nmt=18)


![[카드뉴스] 국립생태원과 함께 환경보호 활동 강화하는 KT&G](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=202403221529138957c1c16452b0175114235199_0.png&nmt=18)
![[카드뉴스] 신생아 특례 대출 조건, 한도, 금리, 신청방법 등 총정리...연 1%대, 최대 5억](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=20240131105228940de68fcbb35175114235199_0.jpg&nmt=18)
![[신간] 리빌딩 코리아 - 피크 코리아 극복을 위한 생산성 주도 성장 전략](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2025032814555807705f8caa4a5ce12411124362.jpg&nmt=18)
![[신간] 지속 가능 경영, 보고와 검증](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2025011710043006774f8caa4a5ce12411124362.jpg&nmt=18)
![[서평] 추세 매매의 대가들...추세추종 투자전략의 대가 14인 인터뷰](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2023102410444004986c1c16452b0175114235199.jpg&nmt=18)

![[신간] 똑똑한 금융생활...건전한 투자와 건강한 재무설계 지침서](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2025031015443705043c1c16452b012411124362.jpg&nmt=18)

![[카드뉴스] KT&G ‘Global Jr. Committee’, 조직문화 혁신 방안 제언](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=89&h=45&m=1&simg=202503261121571288de68fcbb3512411124362_0.png&nmt=18)
![[AD] 기아, 혁신적 콤팩트 SUV ‘시로스’ 세계 최초 공개](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=89&h=45&m=1&simg=2024123113461807771f9c516e42f12411124362.jpg&nmt=18)
![[AD] 아이오닉5 '최고 고도차 주행 전기차' 기네스북 올랐다...압도적 전기차 입증](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=89&h=45&m=1&simg=2024123113204707739f9c516e42f12411124362.jpg&nmt=18)




