유한양행의 비소세포폐암 치료제 ‘렉라자(성분명 레이저티닙)’가 미국 식품의약품청(FDA) 승인을 받았다. 이번 승인은 국내 최초 미국 시판 허가를 받은 기념비적인 사례로, 세간의 이목을 한 몸에 받고 있다. 유일한 박사의 오랜 창업이념이 반영된 결실이라는 평가가 뒤따른다.
유한양행은 ‘털어서 먼지 하나 나오지 않는 기업’으로도 유명하다. 이는 창업주인 유일한 박사의 신념이 반영됐다.
미국에서 잘나가는 사업가였던 유일한 박사는 1926년 한국으로 와 제약회사를 세울 결심을 한다. 과거 사업차 중국 북간도에 갔다가 우리 민족들이 굶주리거나 병에 걸려 죽는 것을 본 후에 내린 결정이었다. 당시 그가 미국에서 들고 온 짐의 대부분은 약품일 정도로 우리 민족의 건강 향상이 가장 큰 관심사였다.
이후 유일한 박사가 설립한 유한양행은 1933년 진통소염제 안티푸라민을 개발해 판매했고, 당시 이 약은 가정상비약으로 많은 인기를 끌었다.
이런 가운데 유일한 박사는 윤리경영을 중시하며 불법경영과 탈세를 단 한 번도 하지 않은 것으로 전해진다.
특히 유일한 박사는 기업에서 일어나는 친인척 분쟁을 막기 위해 경영권을 전문경영인에게 승계하도록 했다. 세상을 떠날 때는 전 재산을 사회에 환원하며 남은 자식에게 일절 재산을 물려주지 않았다.
유일한 박사의 창업이념을 계승함에 따라 유한양행은 ‘주인 없는 기업’으로 운영됐다. 하지만 임직원 모두가 한마음 한뜻으로 움직이며 국내 최초 항암제 FDA승인이라는 결실을 맺게 됐다. 회사의 주인은 구성원이며 회사에서 가장 중요한 자원은 사람이라는 인간존중의 기업문화가 잘 실천돼온 덕분이다.
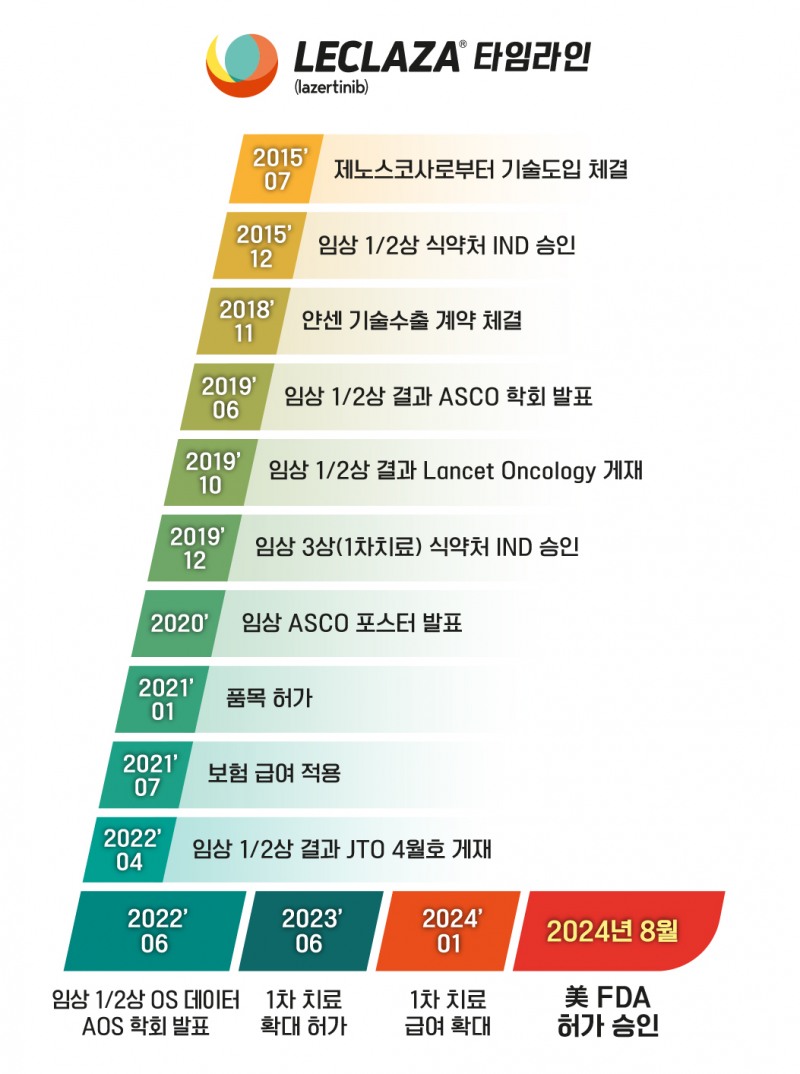
렉라자(레이저티닙)는 유한양행이 국산 신약 31호로 개발한 폐암 치료제다. 비소세포폐암 치료제 ‘렉라자’(레이저티닙)와 글로벌 제약사 존슨앤드존슨(J&J)의 항암제 ‘리브리반트’(아미반타맙)의 병용 요법이 FDA로부터 승인을 받았다.
이를 통해 유한양행은 얀센으로부터 약 800억원 규모의 마일스톤(단계별 기술료)을 수령하게 되며 초소 10% 이상의 제품 판매 로열티도 받게 된다.
이번 승인으로 렉라자·리브리반트 병용요법은 EGFR 변이 NSCLC 환자의 1차 치료제 중 최초이자 유일한 다중 표적, 비화학요법 병용요법이 됐다. 오시머티닙 단독요법보다 질병 진행 또는 사망위험이 30% 감소시켰고, 무진행 생존기간(PFS)은 23.7개월이다. 오시머티닙의 16.6개월 보다 길었으며 반응 지속 기간(DOR)도 25.8개월로 오시머티닙의 16.8개월보다 9개월 더 긴 것으로 나타났다.
요법의 희소성과 우수한 효능으로 렉라자·리브리반트 병용요법은 승인 전부터 매출에 대한 기대감이 높다. 특히 폐암은 전 세계에서 가장 많이 발생하는 암종이며 그 중에서도 NSCLC는 전체 폐암의 80~85%에 해당하는 매우 흔한 암이다. 이 가운데 해당 요법이 타깃하는 EGFR 돌연변이는 전체 NSCLC 중 30~40% 사례에서 관찰되는 매우 흔한 유전자 변이암이다.
유한양행의 FDA승인 소식이 알려진 21일 주가는 전일대비 5200원(5.53%) 오른 9만9200원에 거래됐다. 특히 장중 10만700원까지 오르며 52주 신고가를 경신했다.
조욱제 유한양행 사장은 “렉라자의 FDA의 승인은 오픈이노베이션을 통한 유한양행 R&D투자의 유의미한 결과물”이라며 “이번 승인이 종착점이 아닌 하나의 통과점이 되어 R&D투자를 통해 한국을 대표하는 글로벌 혁신신약 출시와 함께 유한양행의 Global Top 50 달성을 위한 초석이 됐으면 한다”고 말했다.
박슬기 한국금융신문 기자 seulgi@fntimes.com

































![[DCM] SK렌터카, 유동성 리스크 차단...투자자 반응 기대](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2024103012533004870a837df649411612622953.jpg&nmt=18)



![[DCM] ‘독이 된 사업 확장’ 코리아세븐, ‘온∙오프’ 경쟁 모두 밀려](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2024103013585409982a837df649411612622953.jpg&nmt=18)
![[DCM] 10월 공모채 발행 8조 돌파...기준금리 인하 효과 '톡톡'](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=69&h=45&m=5&simg=2024103019030003030a837df649411612622953.jpg&nmt=18)
















![[카드뉴스] 국립생태원과 함께 환경보호 활동 강화하는 KT&G](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=202403221529138957c1c16452b0175114235199_0.png&nmt=18)
![[카드뉴스] 신생아 특례 대출 조건, 한도, 금리, 신청방법 등 총정리...연 1%대, 최대 5억](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=20240131105228940de68fcbb35175114235199_0.jpg&nmt=18)
![[카드뉴스] 어닝시즌은 ‘실적발표기간’으로](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=298&h=298&m=1&simg=202311301105084674de68fcbb35175114235199_0.png&nmt=18)
![[신간] 사모펀드 투자와 경영의 비밀](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2024102809331308730f8caa4a5ce175114235199.jpg&nmt=18)
![[신간]퍼스널브랜딩, 문학에서 길을 찾다](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2024102214123606876f8caa4a5ce175114235199.jpg&nmt=18)
![[서평] 추세 매매의 대가들...추세추종 투자전략의 대가 14인 인터뷰](https://cfnimage.commutil.kr/phpwas/restmb_setimgmake.php?pp=006&w=81&h=123&m=5&simg=2023102410444004986c1c16452b0175114235199.jpg&nmt=18)









